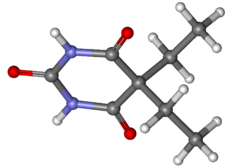
باربيتال
الباربيتال (باللاتينية: Barbital) هو مركب على شكل إبر بلورية بيضاء، ذو طعم خفيف المرارة، ينصهر بين 188 - 192 درجة سيليزية، يُستعمل ملحه (بربيتال الصوديوم) مسكناً ومنوماً لأمد قصير، ويسمى أيضاً (بالإنجليزية: diethyl barbituric acid)،[1] وإن الاسم الكيميائي للباربيتال هو ثنائي إيثيل مالونيل اليوريا، أو ثنائي إيثيل حمض الباربيتوريك.
| باربيتال | |
|---|---|
| الاسم النظامي | |
| 5,5-diethylpyrimidine-2,4,6(1H,3H,5H)-trione | |
| اعتبارات علاجية | |
| ASHPDrugs.com | أسماء الدواء الدولية |
| مدلاين بلس | a682221 |
| طرق إعطاء الدواء | Oral |
| بيانات دوائية | |
| عمر النصف الحيوي | 30.3 (± 3.2) hours |
| معرّفات | |
| CAS | 57-44-3 |
| ك ع ت | N05N05CA04 CA04 |
| بوب كيم | CID 2294 |
| ECHA InfoCard ID | 100.000.301 |
| درغ بنك | DB01483 |
| كيم سبايدر | 2206 |
| المكون الفريد | 5WZ53ENE2P |
| كيوتو | D01740 |
| ChEBI | CHEBI:31252 |
| ChEMBL | CHEMBL444 |
| بيانات كيميائية | |
| الصيغة الكيميائية | C8H12N2O3 |
| الكتلة الجزيئية | 184.193 g/mol |
| تعديل مصدري - تعديل | |
التحضير
عدلإن أول من اصطنع الباربيتون عام 1902 هما الكيميائيان الألمانيان إيميل فيشر وجوزيف فون ميرينغ، واللذان نشرا اكتشافهما عام 1903، وسوّق إنتاجهما من قبل شركة باير تحت اسم "فيرونال". كما سوّق الملح المنحل للباربيتون من قبل شركة شيرينغ Schering AG تحت اسم ميدينال".
يمكن اصطناع الباربيتون من تفاعل تكاثف اليوريا مع ثنائي إيثيل-2,2-ثنائي إيثيل المالونات، وهو مشتق لمركب ثنائي إيثيل المالونات.
التأثير الدوائي
عدليعد الباربيتون من أحسن المنومات المتوفرة. كان طعمه قليل المرارة، ولكنه أحسن من المذاق غير المقبول للبروميدات. يمتلك الباربيتون بعض التأثيرات الجانبية. جرعته العلاجية بعيدة عن الجرعة السامة. على الرغم من ذلك، فإن الاستخدام المديد ينتج عنه تحمل للدواء، مما يتطلب زيادة في الجرعة للوصول إلى التأثير المطلوب. لذلك فإن الجرعة المفرطة القاتلة لهذا المنوم بطيء التأثير لم تكن غير شائعة. يعد الطيار الرائد آرثر ويتن براون من الشخصيات التي توفيت بجرعة مفرطة مفاجئة.[2]
الاستخدامات
عدلاستخدمت محاليل الباربيتال الصودي بوصفها محاليل موقية في البحوث الحيوية، مثال: التناضح الحلولي المناعي أو في المحاليل المثبتة.[3][4] بما أن الباربيتال مادة يمكن التحكم بها، فالمحلول الوقائي القلوي منها استعيض عنه بمواد أخرى.[5]
المراجع
عدل- ^ معجم مصطلحات الكيمياء (بالعربية والإنجليزية والفرنسية) (ط. 1)، دمشق: مجمع اللغة العربية بدمشق، 2014، ص. 48، OCLC:931065783، QID:Q113378673
- ^ "Arthur Whitten Brown (1886–1948) – Find A Grave Memorial". Findagrave.com. مؤرشف من الأصل في 2016-12-06. اطلع عليه بتاريخ 2014-04-19.
- ^ "Wolf D. Kuhlmann, "Buffer Solutions"" (PDF). 10 سبتمبر 2006. مؤرشف من الأصل (PDF) في 2016-11-09. اطلع عليه بتاريخ 2014-07-28.
- ^ Steven E. Ruzin (1999). Plant Microtechnique and Microscopy. Oxford University Press. مؤرشف من الأصل في 2019-06-03. اطلع عليه بتاريخ 2014-07-28.
- ^ Monthony JF, Wallace EG, Allen DM. (1978). "A non-barbital buffer for immunoelectrophoresis and zone electrophoresis in agarose gels". Clin Chem. ج. 24 ع. 10: 1825–1827.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link)