كتلة جزيئية
الكتلة الجزيئية في الكيمياء لمادة (أحيانا يطلق عليها الوزن الجزيئي للمادة) هي كتلة جزيء من هذه المادة، منسوبة إلى وحدة الكتل الذرية (u والتي تساوي 1\12 من كتلة ذرة ن الكربون-12) (بشكل مبسط: الكتلة الجزيئية عبارة عن مجموع أوزان الذرات في الجزيء).[1][2][3]
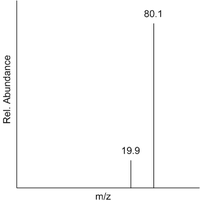
ويمكن حساب الكتلة الجزيئية على أنها مجموع الأوزان الذرية للذرات الموجودة في أي جزيء. كما يمكن قياس الكتلة الجزيئية مباشرة باستخدام مطياف الكتلة. وفي مطياف الكتلة، الكتلة الجزيئية للجزيئات الصغيرة (أقل من تقريبا 200 ذرة لعنصر معين) تكون دقيقة، أي أنها تكون مجموع أكثر نظائر هذا العنصر تواجدا. وللجزيئات الأكبر، فإنها تكون متوسطة، أو يتم حسابها باستخدام الكتلة الجزيئية للعنصر أو باستخدام الجدول الدوري، حيث أنه يوجد إحصائيات لتوزيع الذرات ممثلة نظائر الجزيء.
الكتلة المولية لمادة تساوي عدديا الكتلة الجزيئية، ولكن يعبر عنها بوحدات الكتلة لكل مول، عادة ما تكون g/mol (جرام لكل مول).
- فمثلا:
- الكتلة الذرية للهيدروجين تساوي 1.00784 u وللأكسجين 15.9994 u وحدة كتل ذرية، وعلى هذا، فإن الكتلة الجزيئية للماء والتي لها الصيغة الجزيئية H2O تكون (2 × 1.00784) + 15.9994 = 18.01508 u، حيث هي وحدة الكتل الذرية. وعلى هذا، فإن مول واحد من الماء يزن 18.0150 جرام. وعموما، فإن الكتلة الصحيحة للهيدروجين-1 (أكثر النظائر وجودا) تساوي 1.00783، وللأكسجين-16 (أكثر النظائر وجودا) تساوي 15.9949، وعلى هذا فإن كتلة أكثر جزيئات الماء تواجدا تساوي 18.0105 u.
الكتلة الجزيئية أو الكتلة المولية تستخدم في حسابات الكيمياء الكمية.
وحيث أن الجزيئات تكونت من تفاعل كيميائي، وليس عن طريق تفاعل نووي، فإن الكتلة الجزيئية لجزيء تساوي بالضبط مجموع الأوزان الذرية للذرات المكونة له.
الوزن الجزيئي الجرامي هو الوزن الجزيئي لمركب كيميائي معبرا عنه بالجرامات. وعلى هذا فإن الوزن الجزيئي لكربونات الكالسيوم يساوي 100، ويكون الوزن الجزيئي الجرامي يساوي 100 جرام. ويستخدم الوزن الجزيئي الجرامي خاصة لحساب تركيز المحاليل. وعلى ذلك فإن المحلول المولي يحتوي على الوزن الجزيئي الجرامي لمادة كيماوية مذابة لتحضير لتر من المحلول.
الكتل الجزيئية للغازات
عدللتحديد الكتل الجزيئية للغازات
- الطريقة الأولى
تعتمد على مبدأ افوجادرو «الحجوم المتساوية من الغازات المختلفة تحتوي على نفس العدد من الجزيئات عند نفس الظروف من الضغط ودرجة الحرارة» القانون
حجم الغاز1 = حجم الغاز2
أي ان كثافة الغاز الأول \ كثافة الغاز الثاني = الكتلة الجزيئية للغاز الأول \الكتلة الجزيئية للغاز الثاني
- الطريقة الثانية
تعتمد على معرفة حجم وضغط وكتلة ودرجة حرارة محددة من الغاز المجهول
ح * ض = ن * ك * ت
ح الحجم ض الضغط ن عدد المولات ت درجة الحرارة
مثال الكتلة الجزيئية لملح الطعام
عدلالكتلة الجزيئية (أو كتلة مولية) لملح الطعام (كلوريد الصوديوم):
بتطبيق الكتل الذرية المذكورة في الجدول السابق للكلور 35.453 والصوديوم 22.989 ، نحصل على الكتلة الجزيئية لكلوريد الصوديوم M
u:
- M(NaCl) = [22.989 + 35.453] × 1 g/mol = 58.443 g/mol
انظر أيضًا
عدلمراجع
عدل- ^ Neufeld, R.؛ Stalke, D. (2015). "Accurate Molecular Weight Determination of Small Molecules via DOSY-NMR by Using External Calibration Curves with Normalized Diffusion Coefficients". Chem. Sci. ج. 6: 3354–3364. DOI:10.1039/C5SC00670H.
- ^ Johnson Jr., C. S. (1999). "Diffusion ordered nuclear magnetic resonance spectroscopy: principles and applications". Progress in Nuclear Magnetic Resonance Spectroscopy. ج. 34: 203–256. DOI:10.1016/S0079-6565(99)00003-5.
- ^ الاتحاد الدولي للكيمياء البحتة والتطبيقية (1980). "Atomic Weights of the Elements 1979" (PDF). Pure Appl. Chem. ج. 52 ع. 10: 2349–84. DOI:10.1351/pac198052102349. مؤرشف من الأصل (PDF) في 2018-10-05. نسخة محفوظة 5 أكتوبر 2018 على موقع واي باك مشين.