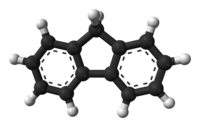
فلورين (مركب كيميائي)
الفلورين هو هيدروكربون عطري متعدد الحلقات له الصيغة الكيميائية C13H10 ويكون على شكل صلب أبيض اللون.
| فلورين[1] | |
|---|---|
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
9H-Fluorene |
|
| تسمية الاتحاد الدولي للكيمياء | |
Tricyclo[7.4.0.02,7]trideca-2,4,6,9,11,13-hexaene |
|
| المعرفات | |
| CAS | 86-73-7 |
| بوب كيم | 6853[2] |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | C13H10 |
| الكتلة المولية | 166.22 غ/مول |
| المظهر | صلب أبيض اللون |
| الكثافة | 1.20 غ/سم3 |
| نقطة الانصهار | 115 °س |
| نقطة الغليان | 295 °س |
| الذوبانية في الماء | عملياً غير منحل في الماء |
| الذوبانية | يذوب في البنزين والإيثر والتولوين |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
يشتق اسم المركب من الخاصة الفلورية، إذ تبدي بلورات هذا المركب وميضاً فلورياً بنفسجياً بالتعرض للأشعة فوق البنفسجية.
الوفرة الطبيعية والتحضير
عدليوجد الفلورين طبيعياً في قطران الفحم، ولكن يمكن الحصول عليه صناعياً من تفاعل نزع هيدروجين من ثنائي فينيل الميثان.[4]
كما يمكن أن يتم التحضير من اختزال مركب فلورينون باستخدام الزنك.[5]
الخواص
عدليوجد الفلورين على شكل بلورات بيضاء غير منحلة عملياً في الماء، ولكنها تنحل في المذيبات العضوية مثل ثنائي كبريتيد الكربون والإيثر الإيثيلي والأسيتون والبنزين والتولوين والبيريميدين.
للمركب بنية مستوية تقريباً،[6] بحيث تكون كل من حلقتي البنزين مشتركة في الاستواء مع ذرة الكربون المركزية (رقم 9).[7]
الاستخدامات
عدليستخدم الفلورين كمادة انطلاق في تحضير المشتقات العضوية المتعلقة، والتي لها العديد من مدالات الاستخدام في صناعة الأصباغ والمبيدات الحشرية.
المراجع
عدل- ^ Merck Index, 11th Edition, 4081
- ^ ا ب ج د FLUORENE (بالإنجليزية), QID:Q278487
- ^ ChEBI release 2020-09-01، 1 سبتمبر 2020، QID:Q98915402
- ^ Karl Griesbaum, Arno Behr, Dieter Biedenkapp, Heinz-Werner Voges, Dorothea Garbe, Christian Paetz, Gerd Collin, Dieter Mayer, Hartmut Höke "Hydrocarbons" in Ullmann's Encyclopedia of Industrial Chemistry 2002 Wiley-VCH, Weinheim. دُوِي:10.1002/14356007.a13_227
- ^ Fittig, Rud. (1873), "Ueber einen neuen Kohlenwasserstoff aus dem Diphenylenketon" Ber. Dtsch. Chem. Ges. volume 6, p. 187.دُوِي:10.1002/cber.18730060169
- ^ D. M. Burns, John Iball, (1954), Molecular Structure of Fluorene Nature volume 173, p. 635. دُوِي:10.1038/173635a0
- ^ R. E. Gerkin, A. P. Lundstedt and W. J. Reppart (1984) Structure of fluorene, C13H10, at 159 K Acta Crystallographica, volume C40, pp. 1892–1894 دُوِي:10.1107/S0108270184009963