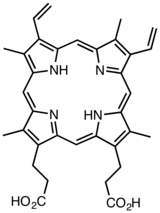
بروتوبورفيرين 9
البروتوبرفيرين 9 هو مركب عضوي من أكثر البورفيرنيات شيوعا في الطبيعة، له لون غامق ولا ينحل بالماء. يوجد البروتوبرفيرين الحر في الطبيعة بشكل معقدات مع الحديد، وعندما يشكل معقدا مع الحديدوز يدعى هيم؛ والهيمات مجموعات ضَميمَة هامة في بعض البروتينات منها هيموغلوبين ومَيوغلوبين وسيتوكروم سي. ويمكن أيضا أن تشكل معقدات مع معادن أخرى مثل الزنك.[1]
| بروتوبورفيرين 9 | |
|---|---|
| أسماء أخرى | |
Protoporphyrin IX |
|
| المعرفات | |
| رقم التسجيل (CAS) | 553-12-8 |
| بب كيم (PubChem) | 4971 |
|
|
|
|
| الخواص | |
| الصيغة الجزيئية | C34H34N4O4 |
| الكتلة المولية | 562.658 g/mol |
| الكثافة | 1.27 g/cm3 |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
البروتوبرفيرين 9 هو جزيء ضخم مستوٍ، فيه مجموعات N-H في وَضع مَفْروق.[2]
الاصطناع الحيوي
عدليتوسَّط الإنزيم بروتوبرفيرين أكسيداز، بحيث يكون الاصطناع الحيويّ المُبَسَّط هو طلائع لا حلقيَّة ← وحيدة البَيرُّول (مُوَلِّد البُرْفوبيلين) ← رُباعيّ البَيرُّول (المعروف أيضًا باسم مُوَلِّد البُرفِيرين (يوروفيرينوجين 3)) ← بورفيرين (البروتوبرفيرين 9).[1]
يعد البروتوبرفيرين 9 طليعة هامة للمجموعات الضَميمَة الأساسية مثل الهيم وسيتوكروم سي والكلوروفيلات، وكنتيجة لذلك تستطيع العديد من الكائنات الحية اصطناع رُباعيّات البَيرُّول هذه ابتداءً من الغليسين أو سَكسينيل التَّميمُ الإِنْزيمِيُّ-أ أو الغلوتامات. وعلى الرغم من كثرة الكائنات التي تصنع البروتوبرفيرين 9 إلَّأ أنَّ العمليَّة محفوظة سواءً في الجراثيم وصولًا إلى الثديات مع وجود بعض الاستثناءات في النباتات العُليا.[3][4][5]
الاصطناع الحيوي للهيم ب واليخضور
عدلفي الاصطناع الحيوي للعوامل المساعدة يُمَعدَن (يُفَلْزَن)البروتوبرفيرين 9 بفعل إنزيمات التَّّمخلُب (المُمَخْلِب)، ويحوِّل الفيرُّوكيلاتاز (إنزيم تمخلب الحديد) البروتوبرفيرين 9 إلى هيم ب (مثل حديد-البروتوبرفيرين 9 أو بروتوهيم 9). وفي الاصطناع الحيوي لليخضور، يحوِّل الإنزيم كيلاتاز المغنزيوم (إنزيم تمخلب المغنزيوم) البروتوبرفيرين 9 إلى مغنزيوم-البروتوبرفيرين 9.
مشتقات الحديد الصناعية
عدليتفاعل بروتوبورفيرين 9 مع أملاح الحديد في الهواء ليعطي المعقّد (FeCl(PPIX.[6]
تسمية البروتوبورفيرين
عدلالبروتوبورفيرينات هي رُباعيّات البَيرُّول الحاوية على أربعة جذور ميثيل وحمضا البروبيونيك وسلسلتا فاينيل جانبيَّة. ويشير العدد 9 الذي يكتب بالأرقام الرُّومانيَّة IX إلى موقع هذه السلاسل الجانبيَّة، لكن تاريخيًّا وضعت التسمية على عدة مراحل.
المراجع
عدل- ^ ا ب Paul R. Ortiz de Montellano (2008). "Hemes in Biology". Wiley Encyclopedia of Chemical Biology. John Wiley & Sons. DOI:10.1002/9780470048672.wecb221.
- ^ Winslow S. Caughey, James A. Ibers (1977). "Crystal and Molecular Structure of the Free Base Porphyrin, Protoporphyrin IX Dimethyl Ester". J. Am. Chem. Soc. ج. 99: 6639–6645. DOI:10.1021/ja00462a027.
- ^ A. R. Battersby؛ C. J. R. Fookes؛ G. W. J. Matcham؛ E. McDonald (1980). "Biosynthesis of the pigments of life: formation of the macrocycle". Nature. ج. 285: 17–21. DOI:10.1038/285017a0.
- ^ F. J. Leeper (1983). "The biosynthesis of porphyrins, chlorophylls, and vitamin B12". Natural Product Reports. ج. 2: 19–47. DOI:10.1039/NP9850200019.
- ^ G. Layer؛ J. Reichelt؛ D. Jahn (2010). "Structure and function of enzymes in heme biosynthesis". Protein Science. ج. 19: 1137–1161. DOI:10.1002/pro.405. PMC:2895239.
- ^ Chang, C. K.؛ DiNello, R. K.؛ Dolphin, D. (1980). "Iron Porphines". Inorg. Synth. Inorganic Syntheses. ج. 20: 147. DOI:10.1002/9780470132517.ch35.