أكونتيز
الأكونتيز: هي عبارة عن ( aconitate الهيدراتيز ) ES(4.2.1.3) وهو انزيم ستيرو محدد للايزومر ويحدث داخل دورة حمض الستريك ويعتبرمن العمليات الغير نشطة للاكسدة.
| aconitate hydratase | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
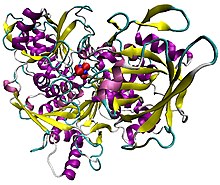 Illustration of pig aconitase in complex with the [Fe4S4] cluster. The protein is colored by secondary structure, and iron atoms are blue and the sulfur red.[1] | |||||||||||
| أرقام التعريف | |||||||||||
| رقم التصنيف الإنزيمي | 4.2.1.3 | ||||||||||
| رقم التسجيل CAS | 9024-25-3 | ||||||||||
| قواعد البيانات | |||||||||||
| قاعدة بيانات الإنزيم | راجع IntEnz | ||||||||||
| قاعدة بيانات براونشفايغ | راجع BRENDA | ||||||||||
| إكسباسي | راجع NiceZyme | ||||||||||
| موسوعة كيوتو | راجع KEGG | ||||||||||
| ميتاسيك | المسار الأيضي | ||||||||||
| بريام | ملف التعريف | ||||||||||
| تركيب بنك بيانات البروتين | RCSB PDB PDBe PDBsum | ||||||||||
| الأونتولوجيا الجينية | AmiGO / EGO | ||||||||||
| |||||||||||
| Aconitase family (aconitate hydratase) | |
|---|---|

| |
| Structure of aconitase.[2] | |
| معرف | |
| رمز | Aconitase |
| قاعدة بيانات عوائل البروتينات | PF00330 |
| إنتربرو | IPR001030 |
| بروسايت | PDOC00423 |
| قاعدة بيانات التصنيف الهيكلي للبروتينات | 1aco |
الشكل البنائي
عدليحتوي على هياكل مختلفة اعتماداً على إذا ما كان نشطاً أو غير نشط ( 6) (7) وينقسم هيكله إلى أربع مجالات
( N_terminal)الطرفية وهي واحدة من الثلاث الأولى المشاركة في التفاعلات مع المجموعة) Fe 4 (Sوأيضاً الموقع النشط يتكون من الوحدات البنائية من جميع المجالات الأربعة بما في ذلك( S_termi(nal الطرفية التي تأخد المجال الأكبر.
كما توجد مجموعات ومنها (Fe_s ( و ((SO 4 في الموقع النشط تعمل على تنشيط الإنزيم فتحصل على ذرة حديد إضافيه فتتكون كتلة من عنصر (Fe_4s ((7)(8) أما بقية الإنزيمات لا تتغير أبدا تبقى محفوظة في نفس الموضع والفرق يكون (0.1 )انجستروم.
الوظيفة
عدلعلى خلاف غالبية البروتينات التي تعمل على حوامل إلكترون فكتلة الحديد والكبريت تتفاعل مباشرة مع الإنزيم. يحتوي الكونتيز على كتلة [fe4S4] ^2 تتحول إلى عنصر (L) غير نشط.
وتشكل الكونتيز التخليق الحيوي لليوسين وهي متجانسات النيوكليتيد وهي 28 عائلة مكونة منIRS) ) وهي عبارة عن تراكيب غير حلقية تنظم تخزين الحديد وتصنيع الهيم وامتصاص الحديد كما أنه يرتبط مع الريبوسوم ويتحكم في دورات الحمض النووي الريبوزي ويرتبط البروتين في 3 و5 من كل المناطق التالية ((IRE_BP . IRES ويتم تثبيط الكونتيز عن طريق الفلوروآسيتيت ( ( fluoroacetate وهي تكون سامة ولا يمكن أن ترتبط بالكونتيز وبالتالي يتم إيقاف حمض الستريك وتعتبر مجموعة الكبريت الحديدية حساسة للغاية بسبب الأكسيد الفائق.
يتم تحرير cis conitate) ) من الإنزيم ويعاد تثبيته في وضع isocitrate) ) لإكمال التفاعل (1 ( وتوجد فرضية أخرى لcis aconitate ) ) يبقى مرتبطا بالإنزيم أثناء تقلبه من الستيرات (10) والكونتيز يحفز القضاء على إزالة أو إضافة الماء وتقوم البقايا السيرين والهستدين بالتعويض عن أعمالها التحفيزية فالهستدين يكون العنصر الأساسي فيقوم باستخراج البروتين من الماء من خلال تهيئة الكينوكليوفيل للهجوم في (c2) ويتم فصل البروتونات بواسطة ثنائي ((cis aconitate لاستكمال الترطيب وينتج( (isocitrate (10)
المراجع
عدل- ^ ببب: 7ACN; Lauble، H.؛ Kennedy، M. C.؛ Beinert، H.؛ Stout، C. D. (1992). "Crystal structures of aconitase with isocitrate and nitroisocitrate bound". Biochemistry. ج. 31 ع. 10: 2735–48. DOI:10.1021/bi00125a014. PMID:1547214.
- ^ ببب: 1ACO; Lauble، H؛ Kennedy، MC؛ Beinert، H؛ Stout، CD (1994). "Crystal Structures of Aconitase with Trans-aconitate and Nitrocitrate Bound". Journal of Molecular Biology. ج. 237 ع. 4: 437–51. DOI:10.1006/jmbi.1994.1246. PMID:8151704.
- PDB: 7ACN; Lauble, H.; Kennedy, M. C.; Beinert, H.; Stout, C. D. (1992). "Crystal structures of aconitase with isocitrate and nitroisocitrate bound". Biochemistry. 31 (10): 2735–48. doi:10.1021/bi00125a014. PMID 1547214.
- PDB: 1ACO; Lauble, H; Kennedy, MC; Beinert, H; Stout, CD (1994). "Crystal Structures of Aconitase with Trans-aconitate and Nitrocitrate Bound". Journal of Molecular Biology. 237(4): 437–51. doi:10.1006/jmbi.1994.1246. PMID 8151704.
- Beinert H, Kennedy MC (Dec 1993). "Aconitase, a two-faced protein: enzyme and iron regulatory factor". FASEB Journal. 7 (15): 1442–9. PMID 8262329.
- Flint, Dennis H.; Allen, Ronda M. (1996). "Iron−Sulfur Proteins with Nonredox Functions". Chemical Reviews. 96 (7): 2315–34. doi:10.1021/cr950041r.
- Beinert H, Kennedy MC, Stout CD (Nov 1996). "Aconitase as Ironminus signSulfur Protein, Enzyme, and Iron-Regulatory Protein". Chemical Reviews. 96 (7): 2335–2374. doi:10.1021/cr950040z. PMID 11848830.
- Robbins AH, Stout CD (1989). "The structure of aconitase". Proteins. 5 (4): 289–312. doi:10.1002/prot.340050406. PMID 2798408.
- Robbins AH, Stout CD (May 1989). "Structure of activated aconitase: formation of the [4Fe-4S] cluster in the crystal". Proceedings of the National Academy of Sciences of the United States of America. 86 (10): 3639–43. doi:10.1073/pnas.86.10.3639. PMC 287193. PMID 2726740.
- Lauble H, Kennedy MC, Beinert H, Stout CD (Mar 1992). "Crystal structures of aconitase with isocitrate and nitroisocitrate bound". Biochemistry. 31 (10): 2735–48. doi:10.1021/bi00125a014. PMID 1547214.
- Gardner, Paul R. (2002). "Aconitase: Sensitive target and measure of superoxide". Superoxide Dismutase. Methods in Enzymology. 349. pp. 9–23. doi:10.1016/S0076-6879(02)49317-2. ISBN 978-0-12-182252-1.
- Takusagawa F. "Chapter 16: Citric Acid Cycle" (PDF). Takusagawa’s Note. The University of Kansas. Archived from the original (PDF) on 2012-03-24. Retrieved 2011-07-10.
- Beinert H, Kennedy MC, Stout CD (Nov 1996). "Aconitase as Ironminus signSulfur Protein, Enzyme, and Iron-Regulatory Protein" (PDF). Chemical Reviews. 96 (7): 2335–2374. doi:10.1021/cr950040z. PMID 11848830.
- PDB: 1C96; Lloyd SJ, Lauble H, Prasad GS, Stout CD (December 1999). "The mechanism of aconitase: 1.8 A resolution crystal structure of the S642a:citrate complex". Protein Sci. 8 (12): 2655–62. doi:10.1110/ps.8.12.2655. PMC 2144235. PMID 10631981.
- Han D, Canali R, Garcia J, Aguilera R, Gallaher TK, Cadenas E (Sep 2005). "Sites and mechanisms of aconitase inactivation by peroxynitrite: modulation by citrate and glutathione". Biochemistry. 44 (36): 11986–96. doi:10.1021/bi0509393. PMID 16142896.
- Lauble H, Stout CD (May 1995). "Steric and conformational features of the aconitase mechanism". Proteins. 22 (1): 1-11. doi:10.1002/prot.340220102. PMID 7675781.
- "Aconitase family". The Prosthetic groups and Metal Ions in Protein Active Sites Database Version 2.0. The University of Leeds. 1999-02-02. Archived from the original on 8 June 2011. Retrieved 2011-07-10.
| أكونتيز في المشاريع الشقيقة: | |
| |