رباعي كلوروبلاتينات البوتاسيوم
مركب كيميائي
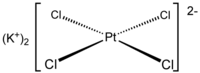
رباعي كلوروبلاتينات البوتاسيوم مركب كيميائي صيغته K2PtCl4، ويوجد في الشروط القياسية على شكل صلب بلوري أحمر اللون.
| رباعي كلوروبلاتينات البوتاسيوم | |
|---|---|
| الاسم النظامي (IUPAC) | |
Potassium tetrachloroplatinate |
|
| أسماء أخرى | |
Potassium chloroplatinite |
|
| المعرفات | |
| CAS | 10025-99-7 |
| بوب كيم | 61440[1]، و3013632، و11069717 |
|
|
| الخواص | |
| الصيغة الجزيئية | K2PtCl4 |
| الكتلة المولية | 415.09 غ/مول |
| المظهر | صلب أحمر |
| الكثافة | 3.4 غ/سم3 |
| نقطة الانصهار | 500 °س |
| الذوبانية في الماء | 0.93 غ/100 مل ماء (عند 16 °س) |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
التحضير
عدليحضر المركب من تفاعل سداسي كلوروبلاتينات البوتاسيوم مع أملاح الهيدرازين (مثل ثنائي كلوريد الهيدرازين).[2]
الخواص
عدليوجد المركب في الشروط القياسية على شكل صلب بلوري أحمر اللون، ينحل بشكل ضعيف في الماء. للبلورات بنية وفق نظام بلوري رباعي، وتتبع الزمرة الفراغية P4/mmm.
يمكن لأيونات الكلوريد في رباعي كلوروبلاتينات البوتاسيوم أن تستبدل بعدة ربيطات في تفاعلات تبادل، كما هو الحال مثلاً في تفاعل تحضير سيسبلاتين.[3]
الاستخدامات
عدليؤدي اختزال رباعي كلوروبلاتينات البوتاسيوم بطرق مناسبة إلى الحصول على فلز البوتاسيوم بحالة غروانية ذات أهمية محتملة في التحفيز الكيميائي.[4]
مراجع
عدل- ^ ا ب ج د Potassium tetrachloroplatinate(II) (بالإنجليزية), QID:Q278487
- ^ Georg Brauer: Handbuch der präparativen anorganischen Chemie. 3., umgearb. Auflage. Band III. Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1712 (بالألمانية)
- ^ Keller, R. N.؛ Moeller, T. (1963). "Potassium Tetrachloroplatinate(II)". Inorg. Synth. Inorganic Syntheses. ج. 7: 247–250. DOI:10.1002/9780470132333.ch79. ISBN:9780470132333.
- ^ Ahmadi, T. S.؛ Wang، Z. L.؛ Green، T. C.؛ Henglein، A.؛ El-Sayed، M. A. (1996). "Shape-Controlled Synthesis of Colloidal Platinum Nanoparticles". ساينس. ج. 272 ع. 5270: 1924ff. DOI:10.1126/science.272.5270.1924. PMID:8662492.